创新医疗器械临床试设计案例-PD-L1 检测试剂盒(免疫组织化学法)
产品名称:PD-L1 检测试剂盒(免疫组织化学法)
企业名称:美国丹科北美有限公司 Dako North America, Inc.
医院数量:3家
临床试验描述:本产品是Dako与百时美施贵宝共同开发的补充诊断产品。 本次申请提交的临床试验,即为共同进行的临床试验包括 Checkmate057国际多中心临床试验及中国人群为主的Checkate 078 临床试验。申请人另外提供了中国境内完成的该试剂与 Ventana公司生产的PD-L1(SP263)试剂的比较研究试验,以及国 内病理医生读片一致性研究。 1.Checkmate057 CheckMate057 是一项 III 期、随机、开放标签、全球多中 心关键研究,评估了纳武利尤单抗 3mg/kg 作为单药治疗既往 铂类双重化疗失败后的晚期或转移性 nsNSCLC 成年受试者(≥18 岁)的安全性和疗效。582 例患者 1:1 接受纳武利尤单抗或多西 他赛治疗。该研究同时对 PD-L1 表达情况与临床效用关系进行 了研究,研究采用申报试剂进行 PD-L1 检测。结果显示,纳武 — 23
— 利尤单抗组中所有 PD-L1 表达患者(按照预定表达水平),其 生存期相较于多西他赛组有所延长,而两组未表达 PD-L1 的患 者的生存期相似。根据 PD-L1 表达水平进行分析时,纳武利尤 单抗亚组中观察到的中位 OS 显著长于多西他赛亚组。PD-L1 表 达水平分别为≥1%、≥5%和≥10%的纳武利尤单抗受试者的中位 OS 分别为 17.1、18.2 和 19.4 个月,而多西他赛受试者的中位 OS 则分别为 9.0、8.1 和 8.0 个月。两个治疗组之间表达水平 <1%、<5%和 <10%的受试者的 OS 并无差异,纳武利尤单抗组的 中位OS范围介于9.7 - 10.4个月之间,而多西他赛组介于 10.1 - 10.3 个月之间。未分层的风险比(HR)和中位总生存期(OS) 见图 2。不同 PD-L1 表达水平亚组的 Kaplan-Meier 曲线见图 3 和图 4。 图2:森林图-nsNSCLC患者不同PD-L1表达量的OS-CheckMate057
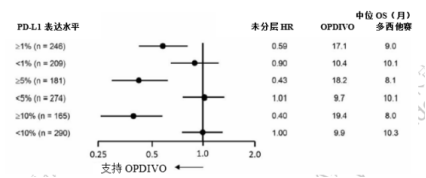
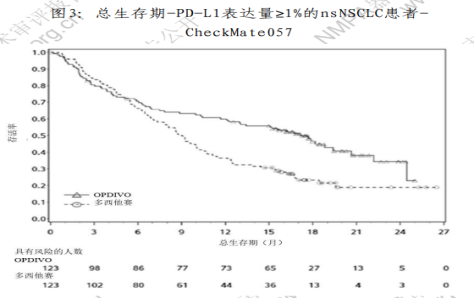
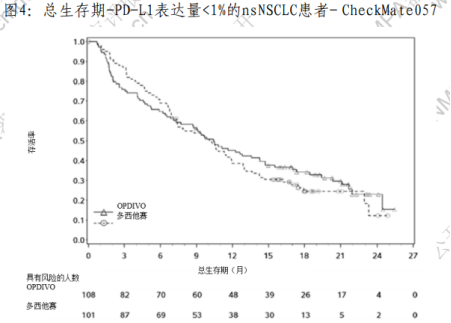
2. Checkmate078 CheckMate078 是一项 III 期、随机、开放标签、亚太区域 (中国为主)的国际多中心临床研究,入组在既往应用含铂剂 二联化疗方案治疗期间或之后发生疾病进展的晚期或转移性 NSCLC 患者。受试者以组织学(鳞状 200 例 vs 非鳞 304 例状)、 PD-L1 状态(阳性 vs 阴性/无法评价)和 ECOG PS(0 vs 1)为 — 26 — 分层因素,以 2:1 比例随机分配至纳武利尤单抗 3 mg/kg IV 每 2 周一次或多西他赛 75mg/m2 IV 每 3 周一次,直疾病进展 或不可耐受,以评价纳武利尤单抗对比多西他赛作为晚期 NSCLC 二线治疗的有效性和安全性。共随机 504 名受试者,分 别接受纳武利尤单抗 3mg/kg (n=338)或多西他赛(n=166)治疗。 根据 OS 的中期分析结果,在预先设定的中期分析即观察到 301 个事件(占最终 OS 分析计划事件数的 79%)时,相较于多 西他赛组,随机至纳武利尤单抗组患者的总生存期有统计学意 义的改善。最短随访 8.8 个月时,纳武利尤单抗组的总生存期 优于多西他赛组,风险比(HR)为 0.68[95% CI:0.54, 0.87], 分层对数秩检验 p 值为 0.0017。纳武利尤单抗组和多西他赛组, 纳武利尤单抗组的总生存期优于多西他赛组,风险比(HR)为 0.76[95% CI:0.56, 1.04],中位 OS 分别为 11.99 个月(95%CI: 10.35-14.00)和 9.63 个月(95% CI:7.62-11.24)。非鳞癌 亚组纳武利尤单抗组和多西他赛组的中位 OS 分别为 11.86 个月 (95%CI:9.40-15.31)和 10.22 个月(95%CI 7.82-12.25), 结果与全球研究 CheckMate057 的趋势一致。 通过 PD-L1 检测试剂盒(免疫组织化学法)检测的肿瘤 PD-L1 表达水平在两个治疗组(纳武利尤单抗组相对于多西他 赛)间均衡。在预设的 PD-L1 表达的亚组分析中,以表达≥1%为 — 27 — cut-off 值,在 PD-L1 阳性受试者中,患者接受纳武利尤单抗组 的获益显著优于多西他赛,HR=0.62,p<0.05,两组的中位 OS 分别为 12.3 月和 7.9 月;在 PD-L1 阴性的患者中,两组 OS 分 别为 11.4 和 10.3 月,HR=0.75,p>0.05。非鳞癌亚组中,以 表达≥1%为 cut-off 值,在 PD-L1 阳性受试者中,患者接受纳武 利尤单抗组的获益优于多西他赛,HR=0.81;在 PD-L1 阴性的患 者中,HR=0.91,纳武利尤单抗组的获益不显著。 3.比较研究试验: 申请人在中国医学科学院北京协和医院、浙江省肿瘤医院 和南京医科大学第一附属医院,共入组 1071 例有效样本(包括 NSCLC,其它癌旁组织和良性疾病或恶性肿瘤),与 Ventana 公 司生产的 PD-L1(SP263)试剂检测结果进行比较研究试验。 除 NSCLC 以外的 152 例其它样本,两种试剂检测结果显示, 阳性符合率为 97.83%,阴性符合率为 100%,总符合率为 99.34%。 Kappa 值为 0.9843,95%置信区间为(0.9537,1.0000)。 919 例 NSCLC 样本,按照临界值 1%的统计结果显示,阳性 符合率为 91.22%,阴性符合率为 97.44%,总符合率为 97.39%。 Kappa 值为 0.9476,95%置信区间为(0.9268,0.9683)。 其中 660 例 nsNSCLC 样本,按照临界值 1%的统计结果显示, 阳性符合率为 95.61%,阴性符合率为 96.98%,总符合率为 — 28 — 96.36%。Kappa
值为 0.9264,95%置信区间为(0.8976,0.9553)。 4.国内病理医生读片一致性研究: 申请人通过对上述比较研究试验过程中,病理医生培训、 环形比对试验和比较研究试验中部分样本的不同病理医生读片 数据,进行分析总结,形成国内病理医生读片一致性分析报 告。 4.1 病理医生培训:本次参与国内临床试验读片的病理医 生均按统一方案接受了规范化培训,使其能准确地对染色样本 进行评分。来自上述 3 家医院的 8 名病理医生经过培训,对 30 个不同 NSCLC 病例(包括 13 例 nsNSCLC 样本)进行评分,其中 第 1 天,对 20 个 NSCLC 病例进行评分。第 2 天,对 25 个病例 进行评分(10 个新病例,15 个第 1 天已经评分后,第 2 天再次 评分)。结果表明病理医生不论资历深浅,对于 NSCLC 或 nsNSCLC 样本,观察员间和观察员内的评分结果具有良好的重 现性(≥85%的一致性)。 4.2 环形比对试验:使用来自 3 家医院的 21 个不同 NSCLC 样本(全部为 nsNSCLC 样本),涵盖 PD-L1 的不同水平。3 家医 院均对切片设盲,按照产品说明书进行染色和读片。所有 3 家 医院 1%临界值的总体一致性为 93.7%。数据表明研究中心间具 有极好的重现性。 — 29 — 3.4 比较研究试验中不同病理医生对同一样本读片一致 性:试验过程中病理医生遇到难以评分的sNSCLC 样本,由第 二名病理医生读片。来源于 3 家医院的 42 份样本分别在各自医 院再次读片,其中 19 例在 1%附近(0.5-10%)。3 家医院共 8 名病理医生对 42 例样本读片,每个样本有 2 个病理医生的读片 结果。数据基于最具挑战性的样本(临界值附近的样本)上分 析得出,总体一致性为 90.5%,证实了观察员间重现性良好。 13 例阴性样本中有 8 例确定为近临界值,即 61.5%。其中 4 例 重复读片不一致的病例中,有 3 例处于近临界值状态,两次阅 片的评分相差仅在 0.5%以内,第 4 个病例的差异为 1%,由于这 几例样本在临界值附件,结果不一致足以影响诊断一致性。 综上所述,该产品临床试验资料对产品的临床性能进行了 较全面研究,临床试验符合要求
【关于我们】
南京西格玛医学技术股份有限公司,总部地处南京,业务覆盖全国。西格玛医学是一家专业从事医疗器械临床研究的创新型CRO,证券代码:873450,致力于为医疗器械提供临床试验专项服务、临床研究、方案撰写、统计分析、数据管理、临床监查、器械SMO、受试者招募、器械第三方稽查和器械注册申报的整体解决方案。
自2009年成立至今,先后更名为南京西格玛咨询中心,南京西格玛医药技术。多年评为江苏高新技术企业,江苏省医疗器械协会会员,通过ISO9001质量体系和多家国内外企业现场认证,和苏州大学,东南大学、南京医科大学成立联合工作站,已成功为遍布25个省份的国内外近千家客户提供专业技术服务,成功完成方案设计撰写、临床监查、数据管理、统计分析、稽查、注册申报等,并建立长期稳定的合作关系。涉及主要的30余个治疗领域,骨科、眼科、肾内科、护理部、整形外科、医疗美容、检验科、ICU、心内科,心外科,病理科、皮肤科等,与全国25个省份近千家医院开展合作,并在国内主要省市设立一站式服务,与全国80%的临床试验机构密切合作,拥有一支稳定并按照国内NMPA、国际标准(ICH-GCP)临床操作的专业团队,具有完整规范详细的标准操作规程(SOP),提供符合NMPA、FDA、EU MDR要求的试验及报告,成功完成NMPA医疗器械Ⅲ类产品临床试验1000余个。项目多次通过国家局、省局和外部审核和稽查。为更好服务和方便客户,我们在全国多个省市开设了上海南格分公司、北京、苏州、西安、长沙、广东等办事处。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼AB座、CD座
电话:025-86210646
手机:同微信13585209568、13913960642
网址:http://www.sigma-stat.com/