创新医疗器械临床试设计案例-人类 SDC2 基因甲基化检测试剂盒(荧光 PCR 法)
产品名称:人类 SDC2 基因甲基化检测试剂盒(荧光 PCR 法)
企业名称:广州市康立明生物科技有限责任公司
医院数量:3家
临床试验描述:申请人在中山大学附属第六医院、南方医科大学南方医 院和山东省肿瘤医院共 3 家临床试验机构完成了临床试验。 14 / 26 采用肠镜(和)或病理的等临床诊断结果为对照方法,通过 与临床参考方法对比验证考核试剂的有效性和安全性,从而 评估考核产品的临床性能。 通过采用单盲、对照的试验设计共筛选入了 1381 例受 试者,有效病例数为 1213 例。其中结直肠癌病例 374 例, 非结直肠癌病例 839 例。结直肠癌病例涵盖了结直肠癌不同 分期的患者,占总入组病例数的 30.83%(374/1213)。非结 直肠癌病例包括干扰人群样本共 551 例,其中含 437 例肠道 相关良性疾病人群样本(主要包括结直肠腺瘤 110 例、结直 肠息肉 114 例、结直肠炎症 151 例、痔疮 47 例以及憩室、 肿物、大肠黑变病、脂肪瘤等)、59 例消化道炎症或肿瘤人 群样本(主要包括胃癌 18 例、食管癌 12 例、胃炎 11 例、 食管炎 8 例以及肝癌、胆管癌、阑尾恶性肿瘤、胰腺癌、喉 鳞癌、十二指肠癌等)、55 例其它肿瘤样本或疾病人群样本 (主要包括黑色素瘤 2 例、神经内分泌癌 5 例、乳腺癌 4 例、 微生物消化道感染 10 例、宫颈癌 1 例、肺癌 6 例、肺鳞癌 8 例、前列腺癌 10 例、类风湿性关节炎 8例以及宫颈鳞癌 1 例)。另外入组 288 例肠道正常人群样本。 将 1213 例有效病例对照方法结果与考核试剂检测结果 进行比较,检测结果如下表所示:
表 2:对照方法与考核试剂检测结果统计四格表
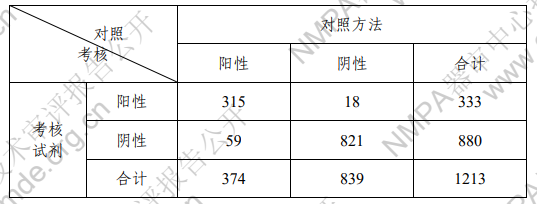
敏感性=A/(A+B)×100%=315/(315+59) ×100%=84.22% 特异性=D/(C+D)×100%=821/(18+821) ×100%=97.85% 总符合率=(A+D)/(A+B+C+D) ×100%=93.65% Kappa=0.85。 临床试验结果显示,1213 例有效病例中,有 77 例样本 考评试剂盒检测结果与对照方法不符,其中假阳性 18 例(主 要集中在肠道相关良性疾病病例,包括息肉 6 例、肠炎 3 例、 重度异型增生 2 例以及腺瘤、胃炎等),假阴性 59 例。对 1213 例有效病例
进行统计分析,结果表明考核试剂对结直肠癌样 本的检测敏感性为 84.22%(315/374),特异性为 97.85% (821/839),总符合率为 93.65%(1136/1213),Kappa 值为 0.85。 对三家临床试验机构入组的 374 例不同分期结直肠癌患 者结果分别进行统计,结果见下表:
表 3:大肠癌临床分期样本检测结果
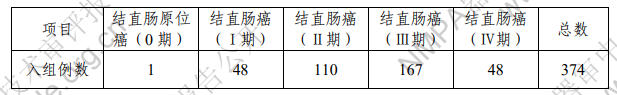

由结果可见,在结直肠癌的不同分期,该指标的检出无 显著差异。 对 77 例考核试剂与对照方法不符的样本和 31 例临床试 验中与对照方法符合的样本(包括肠癌、肠道未见异常、肠 炎、痔疮、息肉、胃癌、食管癌、神经内分泌癌、前列腺癌、 肝癌、肺癌和类分湿性关节炎样本,覆盖了入组临床试验的 各主要样本病例类型)进行测序,结果显示测序结果与试剂 盒检测结果一致性为 100%,说明该产品能够实现对 SDC2 基因甲基化的特异性的检测。 在临床试验中还对 40 例结直肠癌切除根治术前、后的 受试者进行了短期随访。使用考核试剂对符合短期随访要求 的受试者粪便样本进行检测,检测结果显示 39 例检测全为 术前与病理结果相符,术后阴性与结直肠癌手术后的结果相 符。其中有 1 例考核试剂检测结果为样本不合格。 综上所述,考核试剂临床试验对该产品的临床性能进行 了较全面研究,临床试验符合要求
【关于我们】
南京西格玛医学技术股份有限公司,总部地处南京,业务覆盖全国。西格玛医学是一家专业从事医疗器械临床研究的创新型CRO,证券代码:873450,致力于为医疗器械提供临床试验专项服务、临床研究、方案撰写、统计分析、数据管理、临床监查、器械SMO、受试者招募、器械第三方稽查和器械注册申报的整体解决方案。
自2009年成立至今,先后更名为南京西格玛咨询中心,南京西格玛医药技术。多年评为江苏高新技术企业,江苏省医疗器械协会会员,通过ISO9001质量体系和多家国内外企业现场认证,和苏州大学,东南大学、南京医科大学成立联合工作站,已成功为遍布25个省份的国内外近千家客户提供专业技术服务,成功完成方案设计撰写、临床监查、数据管理、统计分析、稽查、注册申报等,并建立长期稳定的合作关系。涉及主要的30余个治疗领域,骨科、眼科、肾内科、护理部、整形外科、医疗美容、检验科、ICU、心内科,心外科,病理科、皮肤科等,与全国25个省份近千家医院开展合作,并在国内主要省市设立一站式服务,与全国80%的临床试验机构密切合作,拥有一支稳定并按照国内NMPA、国际标准(ICH-GCP)临床操作的专业团队,具有完整规范详细的标准操作规程(SOP),提供符合NMPA、FDA、EU MDR要求的试验及报告,成功完成NMPA医疗器械Ⅲ类产品临床试验1000余个。项目多次通过国家局、省局和外部审核和稽查。为更好服务和方便客户,我们在全国多个省市开设了上海南格分公司、北京、苏州、西安、长沙、广东等办事处。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼AB座、CD座
电话:025-86210646
手机:同微信13585209568、13913960642
网址:http://www.sigma-stat.com/
企业名称:
医院数量:
临床试验描述:
【关于我们】
南京西格玛医学技术股份有限公司,总部地处南京,业务覆盖全国。西格玛医学是一家专业从事医疗器械临床研究的创新型CRO,证券代码:873450,致力于为医疗器械提供临床试验专项服务、临床研究、方案撰写、统计分析、数据管理、临床监查、器械SMO、受试者招募、器械第三方稽查和器械注册申报的整体解决方案。
自2009年成立至今,先后更名为南京西格玛咨询中心,南京西格玛医药技术。多年评为江苏高新技术企业,江苏省医疗器械协会会员,通过ISO9001质量体系和多家国内外企业现场认证,和苏州大学,东南大学、南京医科大学成立联合工作站,已成功为遍布25个省份的国内外近千家客户提供专业技术服务,成功完成方案设计撰写、临床监查、数据管理、统计分析、稽查、注册申报等,并建立长期稳定的合作关系。涉及主要的30余个治疗领域,骨科、眼科、肾内科、护理部、整形外科、医疗美容、检验科、ICU、心内科,心外科,病理科、皮肤科等,与全国25个省份近千家医院开展合作,并在国内主要省市设立一站式服务,与全国80%的临床试验机构密切合作,拥有一支稳定并按照国内NMPA、国际标准(ICH-GCP)临床操作的专业团队,具有完整规范详细的标准操作规程(SOP),提供符合NMPA、FDA、EU MDR要求的试验及报告,成功完成NMPA医疗器械Ⅲ类产品临床试验1000余个。项目多次通过国家局、省局和外部审核和稽查。为更好服务和方便客户,我们在全国多个省市开设了上海南格分公司、北京、苏州、西安、长沙、广东等办事处。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼AB座、CD座
电话:025-86210646
手机:同微信13585209568、13913960642
网址:http://www.sigma-stat.com/