创新医疗器械临床试设计案例-miR-92a 检测试剂盒(荧光RT-PCR法)
产品名称:miR-92a 检测试剂盒(荧光RT-PCR法)
企业名称:深圳市晋百慧生物有限公司
医院数量:3家
临床试验描述:申请人在天津市人民医院、深圳市人民医院、中山大学肿瘤防治中心共 3 家临床试验机构完成了临床试验。采用待考核试剂与诊断该疾病的“金标准”全结肠镜诊断检查进行同步比较的方法,验证本产品的临床性能。检测人群包括:通过地方筛查所有便潜血检测阳性患者在临床试验机构进行肠镜检查,同时有阳性患者留取粪便样本采用本试剂盒进行检测。便潜血检测阳性患者共459 例,其中肠镜确诊的大肠癌阳性病例共计 56 例,其余病例为健康人和其他良性疾病者。门诊经临床医生诊断需进行肠镜检查的初诊患者263例,患者症状主要包括排便习惯改变、大便形状变化、大便带血、慢性便秘、排便里急后重等症状。以上所有患者在进行肠镜检查前留取粪便样本采用本试剂盒进行检测,肠镜确诊的大肠癌阳性病例共计 36 例,其余病例为健康人和其他良性疾病患者。大肠癌术前住院患者 248 例,为门诊患者主诉上述症状或其他检查怀疑大肠癌且经肠镜检查确诊为大肠癌,手术前留取患者粪便进行本试剂盒检测。其余病例:其他消化系统肿瘤患者(治疗前)包括食管癌、胃癌、肝癌、胰腺癌、胆管癌、口腔癌,通过病理进 13 / 17 行诊断,于治疗前采集粪便样本进行检测;相关良性疾病患者包括胃炎、肠炎、阑尾炎、结肠炎、消化性溃疡、大肠息肉、腺瘤;以及大肠癌术后住院患者65 例。共入组 1306 例样本,其中以上人群中通过肠镜检查最终确诊为大肠癌的患者共 340 例,通过肠镜确诊为大肠癌阴性的患者 901 例,大肠癌术后患者65 例。同时进行了 179 例样本的测序检测,以验证检测的准确性,测序结果显示检测序列与设计序列一致。临床试验结果: 三家临床试验机构共入组340 例大肠癌患者,采用待考核试剂对不同大肠癌分期患者样本检测结果见表1。
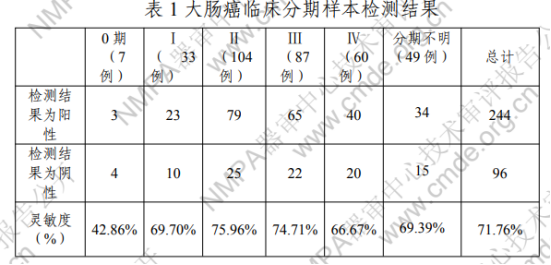
三家临床试验机构共入组59 例腺瘤患者,采用待考核试剂检测结果阳性 8 例,特异性86.44%;共入组20例胰腺癌患者,采用待考核试剂检测结果阳性0 例,特异性100%; 14 / 17 共入组 20 例胆管癌患者,采用待考核试剂检测结果阳性1例,特异性 95.00%;共入组 20 例肝癌患者,采用待考核试剂检测结果阳性 1 例,特异性95.00%;共入组20 例口腔癌患者,采用待考核试剂检测结果阳性1 例,特异性95.00%;共入组 20 例食管癌患者,采用待考核试剂检测结果阳性0例,特异性 100%;共入组 25 例胃癌患者,采用待考核试剂检测结果阳性 2 例,特异性 92.00%。三家临床试验机构共入组45 例肠炎患者,采用待考核试剂检测结果阳性 3 例,特异性93.33%;共入组29例结肠炎患者,采用待考核试剂检测结果阳性2 例,特异性93.10%;共入组 24 例消化性溃疡患者,采用待考核试剂检测结果阳性 1 例,特异性 95.83%;共入组180 例息肉患者,采用待考核试剂检测结果阳性 14 例,特异性92.22%;共入组20例阑尾炎患者,采用待考核试剂检测结果阳性1 例,特异性95.00%;共入组 20 例胃炎患者,采用待考核试剂检测结果阳性 1 例,特异性 95.00%。三家临床试验机构共入组65 例大肠癌术后患者,采用待考核试剂检测结果阳性 11 例,阳性率16.92%。
综合所有试验数据分析,以全结肠镜诊断金标准为参照,本产品检测灵敏度为 71.76%,特异性为90.23%。检测结果与临床诊断金标准符合率较好,结果见表2
表2
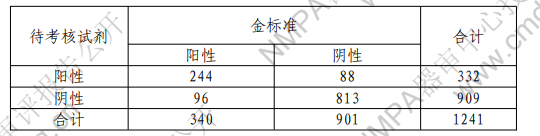
注:65 例术后病例未纳入表中作统计分析。
灵敏度: [244/(244+96)]*100%=71.76%
特异性: [813/(813+88)]*100%=90.23%
【关于我们】
南京西格玛医学技术股份有限公司,总部地处南京,业务覆盖全国。西格玛医学是一家专业从事医疗器械临床研究的创新型CRO,证券代码:873450,致力于为医疗器械提供临床试验专项服务、临床研究、方案撰写、统计分析、数据管理、临床监查、器械SMO、受试者招募、器械第三方稽查和器械注册申报的整体解决方案。
自2009年成立至今,先后更名为南京西格玛咨询中心,南京西格玛医药技术。多年评为江苏高新技术企业,江苏省医疗器械协会会员,通过ISO9001质量体系和多家国内外企业现场认证,和苏州大学,东南大学、南京医科大学成立联合工作站,已成功为遍布25个省份的国内外近千家客户提供专业技术服务,成功完成方案设计撰写、临床监查、数据管理、统计分析、稽查、注册申报等,并建立长期稳定的合作关系。涉及主要的30余个治疗领域,骨科、眼科、肾内科、护理部、整形外科、医疗美容、检验科、ICU、心内科,心外科,病理科、皮肤科等,与全国25个省份近千家医院开展合作,并在国内主要省市设立一站式服务,与全国80%的临床试验机构密切合作,拥有一支稳定并按照国内NMPA、国际标准(ICH-GCP)临床操作的专业团队,具有完整规范详细的标准操作规程(SOP),提供符合NMPA、FDA、EU MDR要求的试验及报告,成功完成NMPA医疗器械Ⅲ类产品临床试验1000余个。项目多次通过国家局、省局和外部审核和稽查。为更好服务和方便客户,我们在全国多个省市开设了上海南格分公司、北京、苏州、西安、长沙、广东等办事处。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼AB座、CD座
电话:025-86210646
手机:同微信13585209568、13913960642
网址:http://www.sigma-stat.com/