急救和转运呼吸机获得NMPA医疗器械注册证
2023年3月18日,深圳哈维生物医疗科技有限公司 的急救和转运呼吸机获得NMPA注册证。本产品预期在专业医疗机构内部或外部进行转运时使用。用于对成人、小儿和婴幼儿进行通气辅助及呼吸支持。本产品应由培训合格获得授权的医务人员进行操作
产品特点体积小、重量轻,配备便携装载平台,方便院内、院外急救使用。支持IV(有创)、NIV(无创)通气模式,性能卓越,操作简单易上手。扩展性强,可配置多种附件模块,支持根据具体使用场景进行功能强化。临床普适院内、院外转运,急救救治,亚危重支持。突破核心技术,拥有自主知识产权的核心控制算法,实现流量、压力和氧浓度的精准控制。对比常见转运呼吸机,E20 EASY的控制更稳定,自耗氧更低,达到世界先进水平。氧浓度40%、100%两档可调,实现幼儿、儿童、成人的多类群体救护。
深圳哈维生物医疗科技有限公司(以下简称:哈维医疗)创立于2019年,是全球领先的呼吸生理和急危重症医疗设备研发制造龙头企业,产品覆盖呼吸和ICU、麻醉和手术室、急救和应急、睡眠和呼吸病及康复健康管理五大业务板块。在中国大陆,哈维医疗业务覆盖全部31个省级行政区域的各级医院,与国内顶尖医疗机构建立起了长期临床合作。此外,哈维医疗积极开拓国际市场,在美国、德国、瑞典、澳大利亚、印尼和印度等地都拥有合作伙伴。在未来的日子里,哈维医疗将持续凭借创新的产品和解决方案,助力构建智慧医院生态体系,融合医工各领域学科,为优质诊疗和医院高效管理赋能。

其中南京西格玛医学技术股份有限公司作为CRO协助撰写临床评价报告。南京西格玛医学技术股份有限公司作为长期合作单位,进行合作,取得了大量的注册证。西格玛医学自2008年开展医疗器械临床试验服务,拥有强大的医学和统计能力团队。自2015年一直开展医疗器械临床评价报告的撰写和评估,公司购买了大量的国内外文献数据库,拥有软件Review Manager、sata、SAS9.4等,可以满足文献查询,资料论证,Meta统计分析等,为众多客户完成了临床评价报告,并取得大量的二三类注册证。同时也开发了医疗器械产品查询数据库,帮助同行更好开展工作。传统临床临床试验耗时费力。采用临床评价,一方面符合CMDE科学性验证体系,确保产品的有效性和安全性;另一方面节省费用,加快产品上市,惠及更多病患。
监管分类:呼吸机类产品按照第Ⅲ类医疗器械管理,附件主要按照第Ⅱ类医疗器械管理,传统临床临床试验耗时费力。采用临床评价,一方面符合CMDE科学性验证体系,确保产品的有效性和安全性;另一方面节省费用,加快产品上市,惠及更多病患。
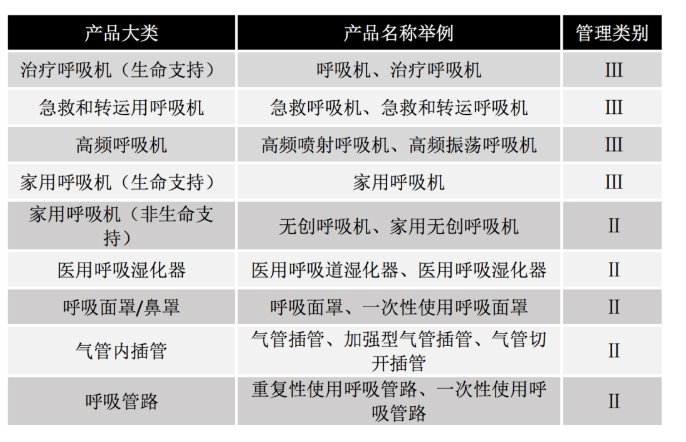
呼吸机上市审批
第Ⅱ、Ⅲ类医疗器械需要注册审批,呼吸机以及附件产品上市前需要取得《医疗器械注册证》和《医疗器械生产许可证》。审批周期为10-12个月(第Ⅱ类)或12-15个月(第Ⅲ类),参考表2。其中呼吸机类产品不在临床试验豁免目录里,还需进行临床试验。
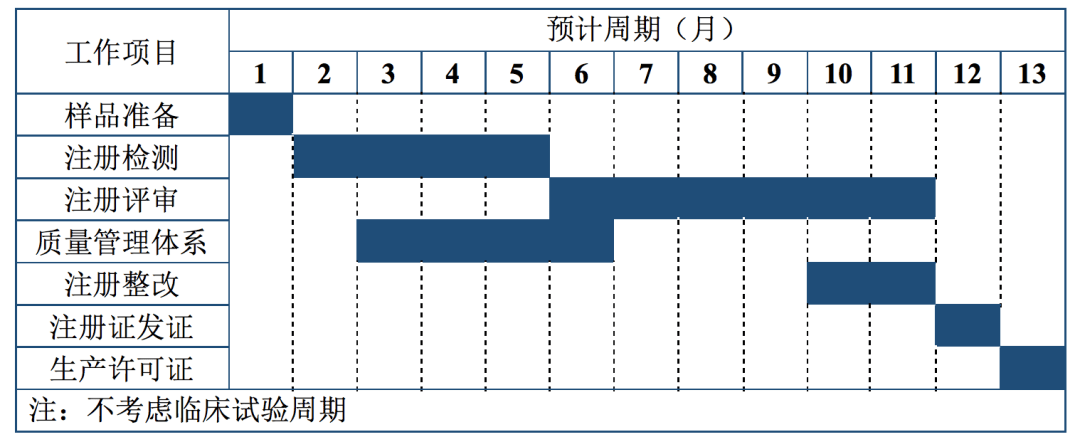
表2 第Ⅱ、Ⅲ类医疗器械产品注册周期参考
医疗器械注册审批流程见图2:
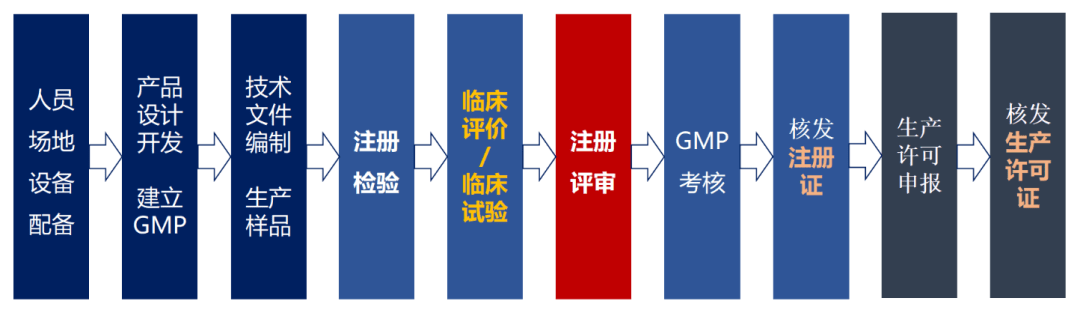
图2 医疗器械注册流程图
医疗器械注册过程中最主要的是注册评审,注册评审阶段的工作以及时间安排见图3。

注册评审阶段周期
市场
呼吸机生产
呼吸机是一个多系统集成的产品,包括外壳、显示器、电路板、压缩机、芯片、传感器、阀门、过滤器、软件等。没有技术基础以及上游供应商的企业无法短期内生产出呼吸机。呼吸机工作原理见图4.
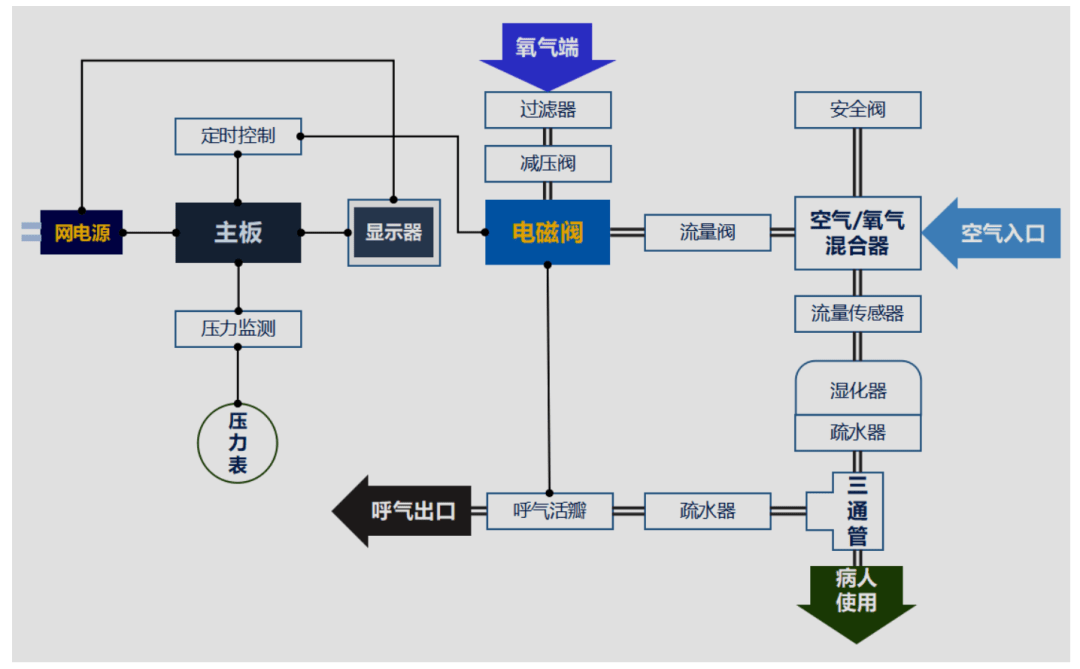
呼吸机工作原理示意图
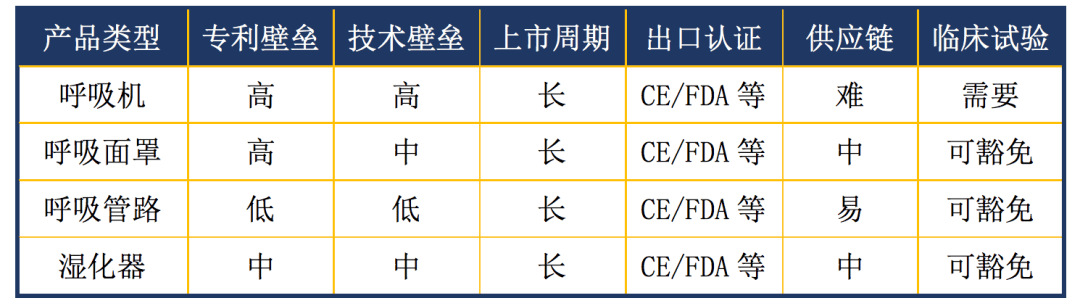
同时,呼吸机及其附件由于高度技术化,新进入的企业面临严重的专利等壁垒,亦无法马上进行相应产品的生产。呼吸机及附件类医疗器械投产的主要难点见表3。
呼吸机类产品生产难度参考
生产企业现状
1) 呼吸机产品中,家用呼吸机市场占有2/3的份额,医用呼吸机占有1/3的市场份额。美国是呼吸机最大的制造和消费市场,其次是欧洲、中国。
2) 中国呼吸机市场上,高端产品主要为国外企业控制。目前中国市场份额最大的是飞利浦伟康(55%)和瑞思迈(25%)。
3) 我国呼吸机产量约占全球产量的1/5,受疫情影响,国内厂家加速生产,产量占比将进一步提高。非疫情情况下,世界主要呼吸机生产和销售地区占比见图5。
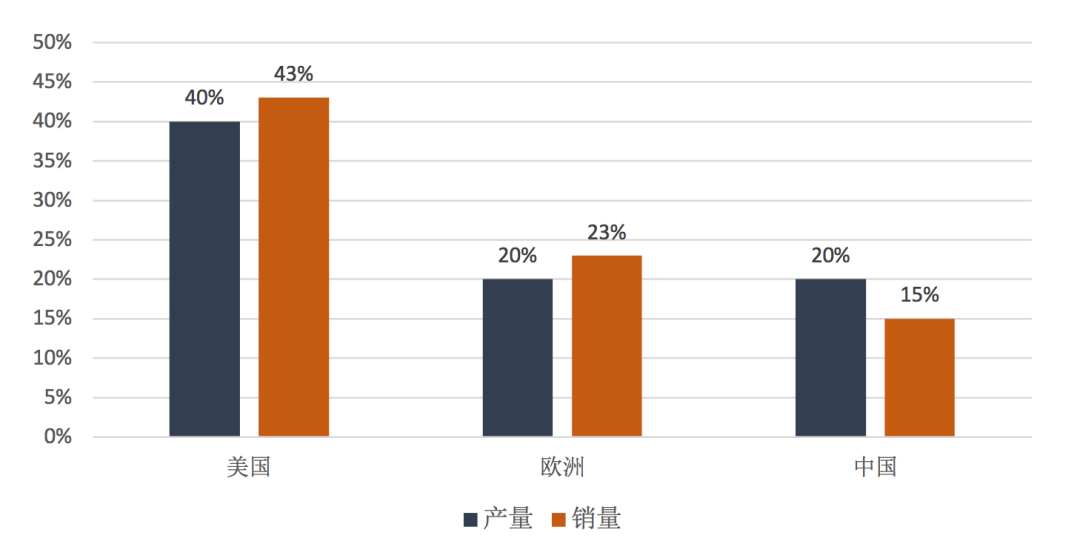
图5 全球各地区呼吸机产销量占比
4) 随着中国市场的需求增大,欧美主要的呼吸机厂家悉数进入中国,同时国内厂家也在快速发展,在占领中低端市场的同时,也在积极研发中高端产品。已取得国内产品注册证的呼吸机厂家。
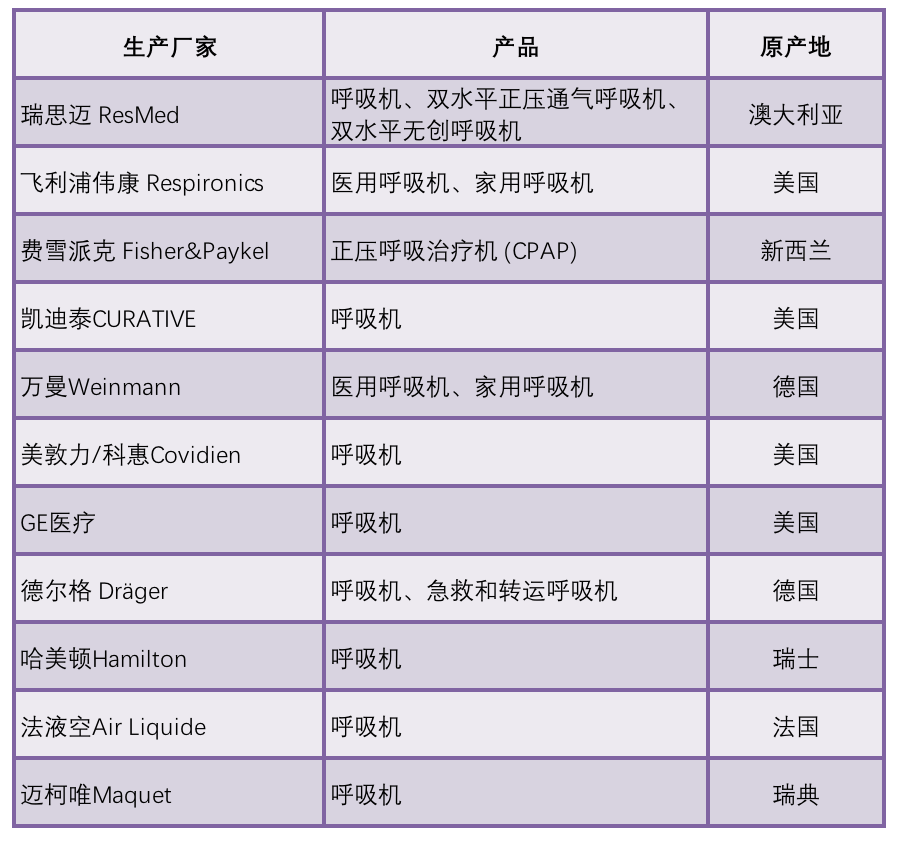
部分进口呼吸机厂家
国内注册呼吸机厂家
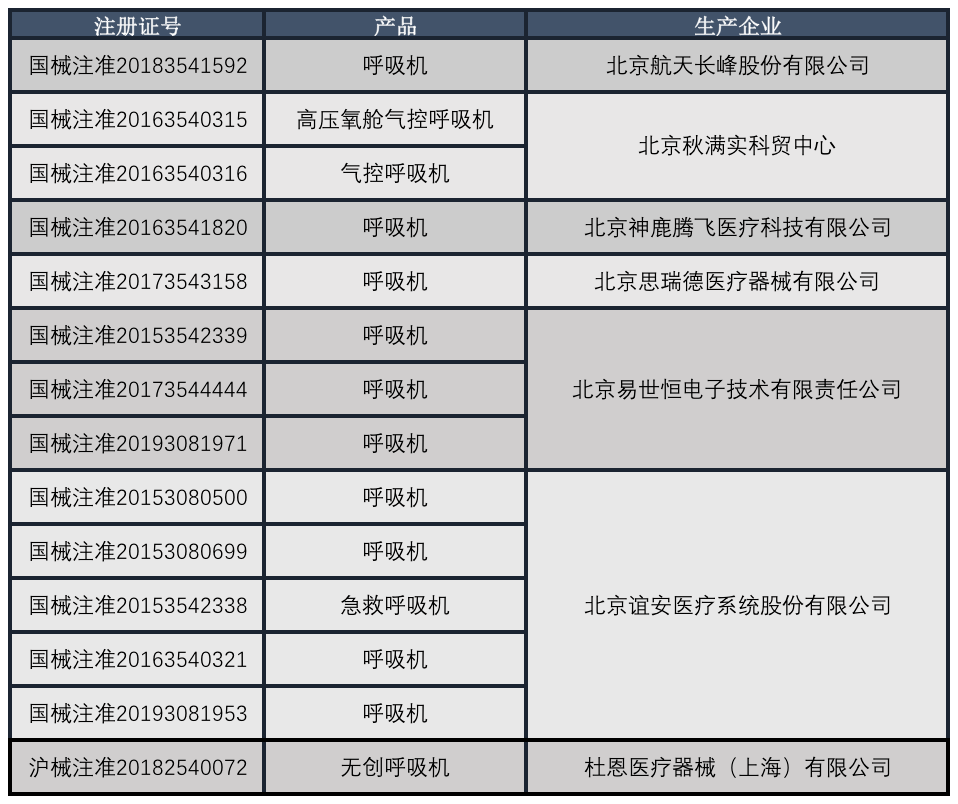
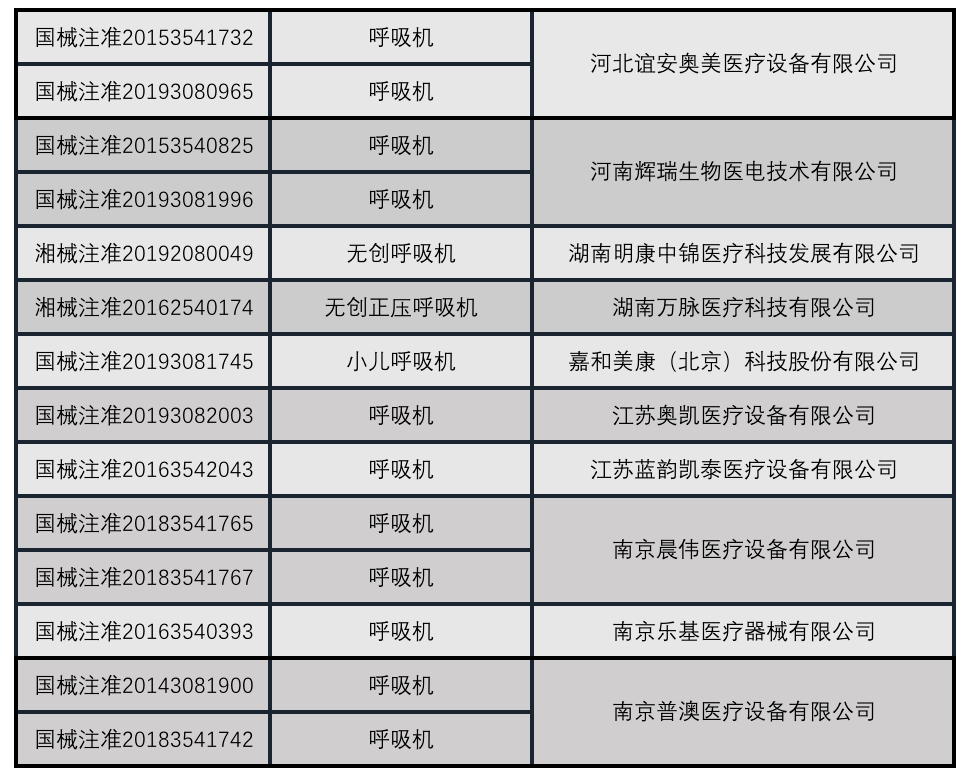
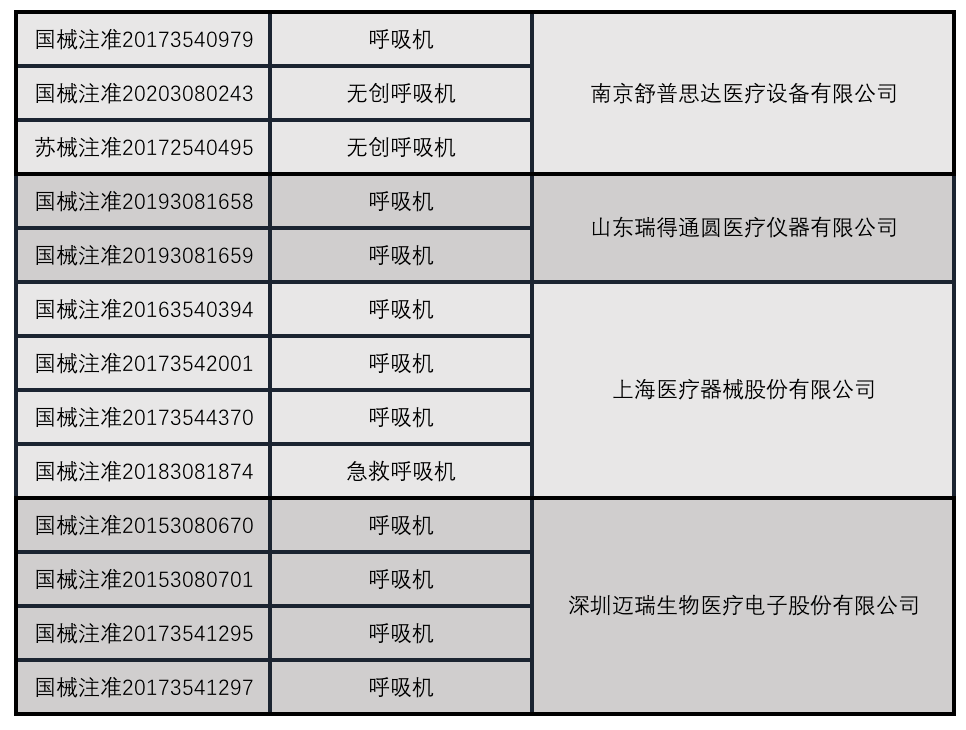
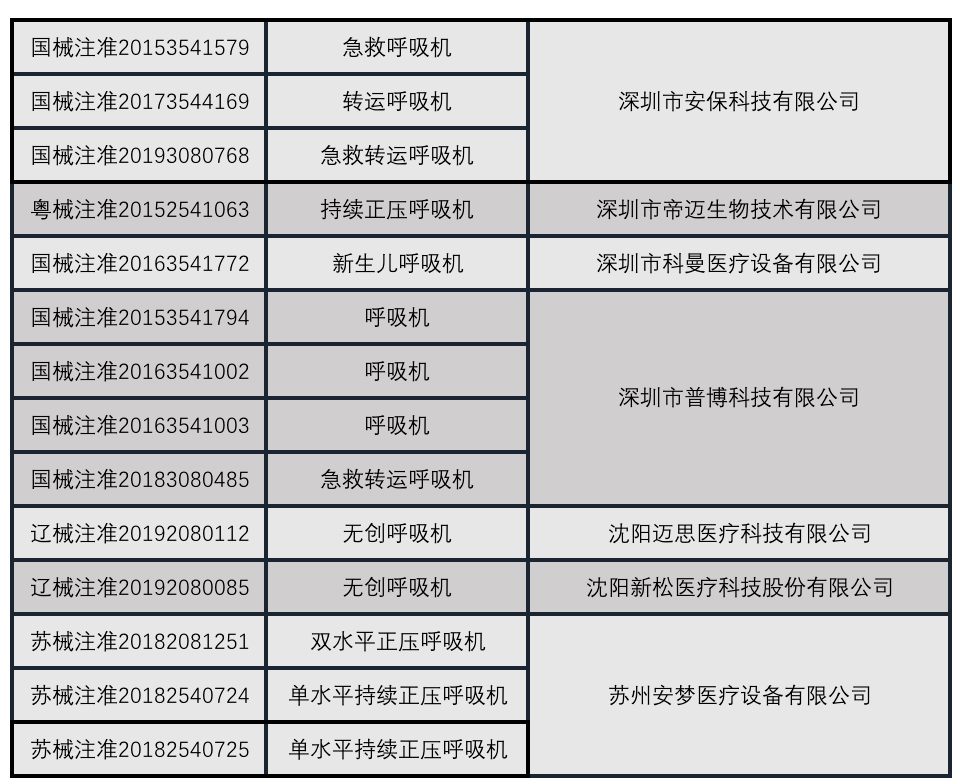
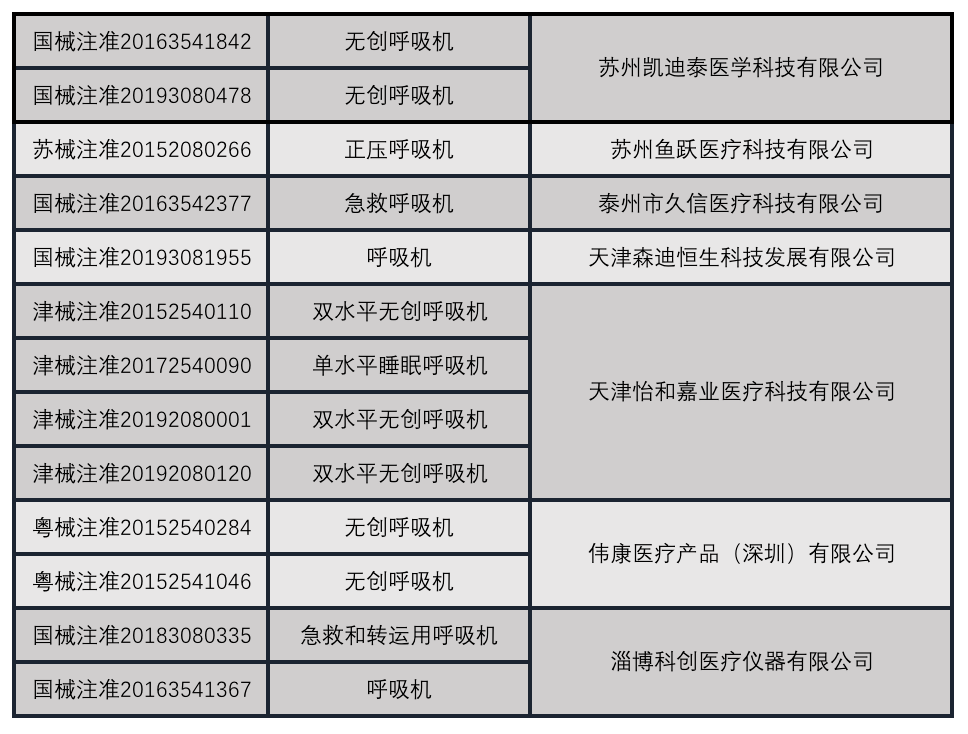
信息来源:NMPA官网
5) 呼吸面罩为呼吸机的主要附件,其在国内的主要生产厂家。
呼吸面罩厂家
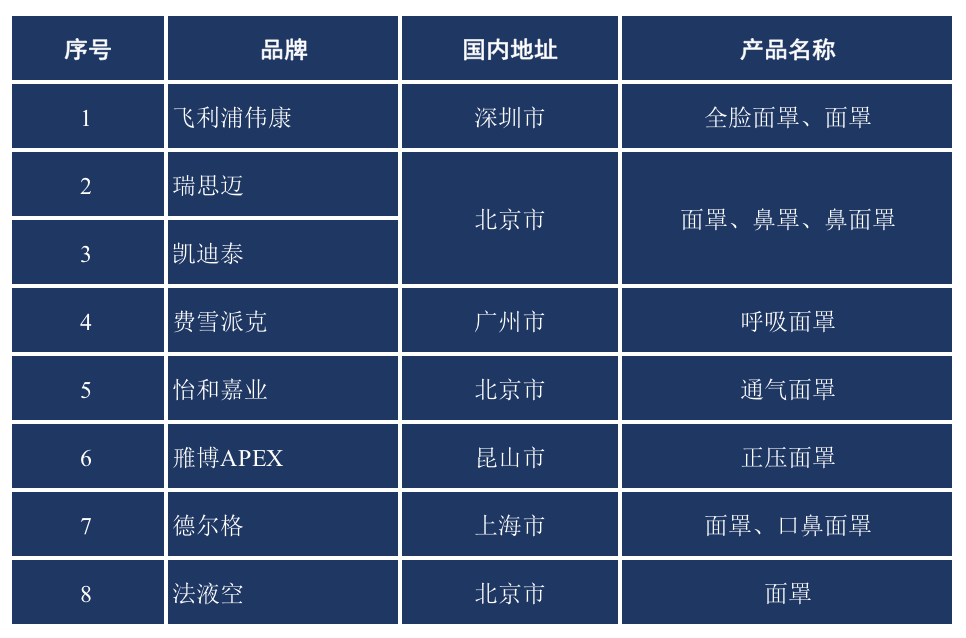
6) 由于技术壁垒和专利壁垒的关系,呼吸面罩产品的市场占有率高度集中,呼吸面罩产品的TOP5企业国内市场占有率高达85%以上。
7) 由于篇幅原因,气管插管、呼吸管路、呼吸湿化器产品不再列举。
建议
1) 自2020年4月1日起,无注册证和生产许可证的防疫医疗器械不得出口。
2) 呼吸机类产品注册周期较长,新企业不宜注册产品。
3) 非生产企业可以考虑销售呼吸机产品、附件、零部件。
4) 销售呼吸机类产品的企业需要办理医疗器械经营许可证、医疗器械经营备案证,受理单位为市级药监部门,流程见表7。
经营企业办证流程


南京西格玛医学技术股份有限公司(SIGMAMED)(873450),地处南京,辐射全国。西格玛医学是一家专业从事医疗器械临床研究的创新型CRO,证券代码:873450,致力于为医疗器械提供临床试验专项服务、临床研究、方案撰写、统计分析、数据管理、监查、器械SMO、受试者招募、第三方稽查和注册申报的整体解决方案。自2009年成立至今,多年评选为江苏省高新技术企业,江苏省医疗器械协会会员,通过ISO9001质量体系和多家国内外企业现场认证,和苏州大学,东南大学、南京医科大学成立联合工作站。西格玛医学已成功为国内外近百家客户提供专业技术服务,成功完成医学方案设计撰写、统计、稽查、临床试验、注册申报等,并建立长期稳定的合作关系。涉及主要的20余个治疗领域,骨科、眼科、肾内、护理、整形美容、IVD、心内科,心外科,皮肤科,普外科等,与全国25个省份近千家医院开展合作,并在国内主要省市设立工作站,与全国80%的临床试验机构密切合作,拥有一支中、高层稳定并按照国际标准(ICH-GCP)操作的专业团队,具有完整规范详细的质量体系和标准操作规程(SOP),成功完成医疗器械Ⅱ、Ⅲ类产品临床试验1000余个。项目多次通过国家局、省局核查和外部公司审核和稽查。为更好服务方便客户,我们特别开设了上海南格、深圳西格玛分公司服务客户。