创新医疗器械临床试设计案例-
产品名称:经导管主动脉瓣膜系统
企业名称:上海微创心通医疗科技股份有限公司
医院数量:第一阶段5家;第二阶段11家
临床试验描述:该临床试验方式为前瞻性、多中心、单组目标值法试验设计, 共分为两个阶段完成,第一阶段纳入 10 例受试者,第二阶段纳 入 110 例受试者验证该产品的安全性及有效性。 临床试验第一阶段主要终点为术后即刻器械成功率,次要终 点为术后手术成功率、术后 30 天的全因死亡率、主要不良事件 发生率。第二阶段主要终点为术后 12 个月全因死亡率,次要终 点为术后即刻器械成功率、术后即刻手术成功率、球囊预扩张 成功率、球囊后扩张成功率、术后即刻/出院前/术后 30 天/6 个月/2~5 年全因死亡率、术后即刻/出院前/术后 30 天/6 个月 /12 个月/2~5 年心肌梗死发生率、出院前/术后 30 天/6 个月/12 个月/2~5 年严重卒中发生率、出院前/术后 30 天/6 个月/12 个 — 21 — 月/2~5 年严重出血、出院前/术后 30 天/6 个月/12 个月/2~5 年 急性肾损伤、术后即刻/出院前手术相关血管并发症、术后即刻 /出院前/术后30天/6个月/12个月/2~5年主要不良心脑血管事 件发生率、术后即刻/出院前/术后 30 天/6 个月/12 个月瓣膜功 能、出院前/术后 30 天/6 个月/12 个月心功能改善、术后 30 天 /6 个月/12 个月生活质量改善。 临床试验第一阶段共 5 家临床机构参与试验,入组受试者 10 例,试验期间术后即刻器械成功率为 90%。详见表 4

次要有效终点指标结果如表 5 所示:术后手术成功率为 90%、 术后 30 天的全因死亡率 20%、主要不良事件发生率 60%。

临床试验第二阶段共 11 家临床机构参与试验,入组受试者 110 例,全分析集(FAS)人群为 110 例,符合方案分析集(PPS) 人群为 109 例。FAS 分析集下试验期间术后 12 个月全因死亡率 为 2.7%,PPS 分析集下术后 12 个月全因死亡率为 2.8%,结果表 明,该临床试验术后 12 个月全因死亡率 95%可信区间满足目标 值的要求。详见表 6。

次要有效性评价指标结果:术后即刻器械成功率为 99.1%、 术后即刻手术成功率为 88.2%、球囊预扩张成功率为 100%、球 囊后扩张成功率为 100%,如表 7 所示,术后即刻/出院前/术后 30 天/6 个月/12 个月瓣膜功能结果如图 2 所示,出院前/术后 30 天/6 个月/12 个月心功能改善结果如图 3 所示、术后 30 天/6 个月/12 个月生活质量改善结果如图 4 所示


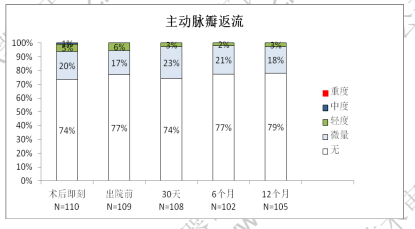
图2 术后即刻/出院前/术后30天/6个月/12个月瓣膜功能结果
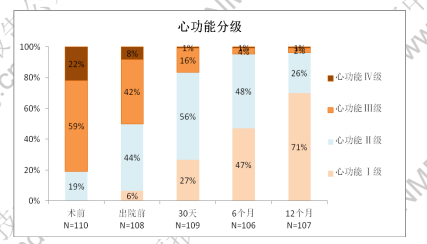
图 3 出院前/术后 30 天/6 个月/12 个月心功能改善结果
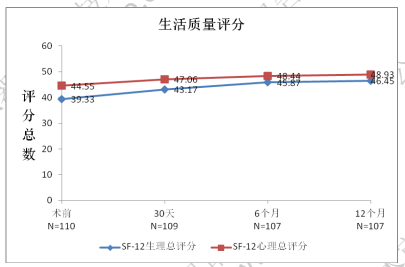
图 4 术后 30 天/6 个月/12 个月生活质量改善结果
主要安全性评价指标结果如表 8 所示:术后 30 天全因死亡 率为 0.9%


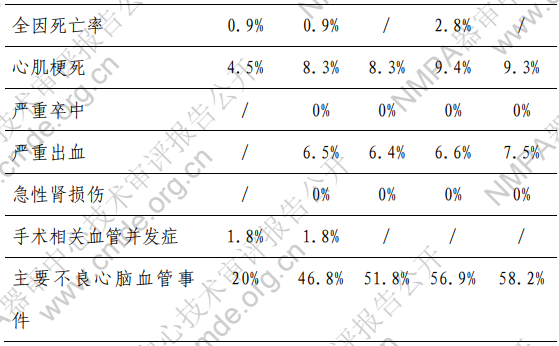
要安全性评价指标结果如表 9 所示:术后即刻和出院前全 因死亡率均为 0.9%、6 个月全因死亡率为 2.8%;术后即刻心肌 梗死发生率为 4.5%、出院前和术后 30 天心肌梗死发生率均为 8.3%、术后 6 个月心肌梗死发生率均为 9.4%、术后 12 个月心肌 梗死发生率均为 9.3%;出院前、术后 30 天、6 个月和 12 个月 的严重卒中发生率均为 0%;出院前严重出血发生率为 6.5%、术 后 30 天严重出血发生率为 6.4%、术后 6 个月严重出血发生率为 6.6%、术后 12 个月严重出血发生率为 7.5%;出院前、术后 30 天、6 个月和 12 个月的急性肾损伤发生率均为 0%;术后即刻和 出院前手术相关血管并发症发生率均为 1.8%;术后即刻主要不 良心脑血管事件发生率为 20%、出院前主要不良心脑血管事件发 生率为 46.8%、术后 30 天主要不良心脑血管事件发生率为 51.8%、术后 6 个月主要不良心脑血管事件发生率为 56.9%、术 后 12 个月主要不良心脑血管事件发生率为 58.2%。

该产品在临床应用中通过经导管方式将人工心脏瓣膜置入 于病变部位,代替原生病变瓣膜工作,解除病变部位狭窄,从 而保证主动脉血流畅通,改善心功能,达到治疗重度主动脉瓣 狭窄目的。但可能伴随卒中、冠脉闭塞、心律失常、血管并发 症等风险。根据申请人提供的申报资料,经综合评价,在目前 认知水平上,认为该产品为患者带来的受益大于风险。
【关于我们】
南京西格玛医学技术股份有限公司,总部地处南京,业务覆盖全国。西格玛医学是一家专业从事医疗器械临床研究的创新型CRO,证券代码:873450,致力于为医疗器械提供临床试验专项服务、临床研究、方案撰写、统计分析、数据管理、临床监查、器械SMO、受试者招募、器械第三方稽查和器械注册申报的整体解决方案。
自2009年成立至今,先后更名为南京西格玛咨询中心,南京西格玛医药技术。多年评为江苏高新技术企业,江苏省医疗器械协会会员,通过ISO9001质量体系和多家国内外企业现场认证,和苏州大学,东南大学、南京医科大学成立联合工作站,已成功为遍布25个省份的国内外近千家客户提供专业技术服务,成功完成方案设计撰写、临床监查、数据管理、统计分析、稽查、注册申报等,并建立长期稳定的合作关系。涉及主要的30余个治疗领域,骨科、眼科、肾内科、护理部、整形外科、医疗美容、检验科、ICU、心内科,心外科,病理科、皮肤科等,与全国25个省份近千家医院开展合作,并在国内主要省市设立一站式服务,与全国80%的临床试验机构密切合作,拥有一支稳定并按照国内NMPA、国际标准(ICH-GCP)临床操作的专业团队,具有完整规范详细的标准操作规程(SOP),提供符合NMPA、FDA、EU MDR要求的试验及报告,成功完成NMPA医疗器械Ⅲ类产品临床试验1000余个。项目多次通过国家局、省局和外部审核和稽查。为更好服务和方便客户,我们在全国多个省市开设了上海南格分公司、北京、苏州、西安、长沙、广东等办事处。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼AB座、CD座
电话:025-86210646
手机:同微信13585209568、13913960642
网址:http://www.sigma-stat.com/