创新医疗器械临床试设计案例-复合疝修补补片
产品名称:复合疝修补补片
企业名称:上海松力生物技术有限公司
医院数量:3家
临床试验描述:该产品以临床试验方式进行临床评价。临床试验目的为评价申报产品用于开放式腹股沟疝无张力修补的安全性及有效性。临床试验为前瞻性、单盲、多中心、随机对 照的非劣效临床试验设计。对照产品为生物疝修补补片(国 食药监械(进)字 2014 第 3463414 号)。 (二)临床试验机构为:复旦大学附属华东医院(组长 单位)、同济大学附属上海市第十人医院、上海中医药大 学附属普陀区中心医院。 (三)有效性评价指标:1.主要终点:有效率。有效率 =1-复发率。复率=复发例数/总的研究例数×100%。2.次要 终点:1)疼痛; 2)不适感; 3)感觉缺失或感觉异常;4) 手术部位迟发性感染的发生率。 (四)安性评价指标:一般体检、生命体征(血压、 心率、呼吸、体温)、实验室检查、心电图检查、B 超检查、 10/15 不良事件、合并用药。其中免疫学指标:CD3、CD4、CD8 细胞百分率,CD4/CD8 细胞比值,免疫球蛋白 IgG、IgM、 IgE、C 反应蛋白(CRP)、补体 C3、C4。 (五)本研究计划入组 188 例,实际入组 172 例,实际收到病例报告表 172 份。未完成病例 3 例,从 PPS 剔除。FAS 数据集人数为 172 例,PPS数据集人数为 169 例,SS 数据集 人数为 172 例。FAS 集疗效结果采用最后一次观察结果结转。 术后 6 个月没有观察到受试者复发,试验组和对照组率差 95%可信区间(FAS(-4.3%~4.3%),PPS(-4.3%~4.4%)) 下限大于预先设定非劣界值-10%,由此可得试验组治疗 6 个 月后有效率非劣于对照组。 术后 33 个月共随访到 157 例受试者,其中试验组 78 例, 对照组 79 例,纳入术后随访的 PPS 集,所有 172 例随机化 受试者纳入 FAS 集,FAS 集疗效结果采用最后一次观察结果结转。试验组复发为 0 例,有效率为 100%(95.38%~ 100.00%);对照组复发 2 例,有效率为 97.46%(91.15%~ 99.69),组间差异没有统计学意义,有效率差值 95%置信区 间为-0.93%~6.00%,下限>非劣界值(-10%),非劣效成立。 临床试验主要/次要评价指标结果见表 5。(六)临床安全性评价指标结果见表 6。试验组和对照 组免疫学观察指标、手术后并发症等指标无统计学差异。
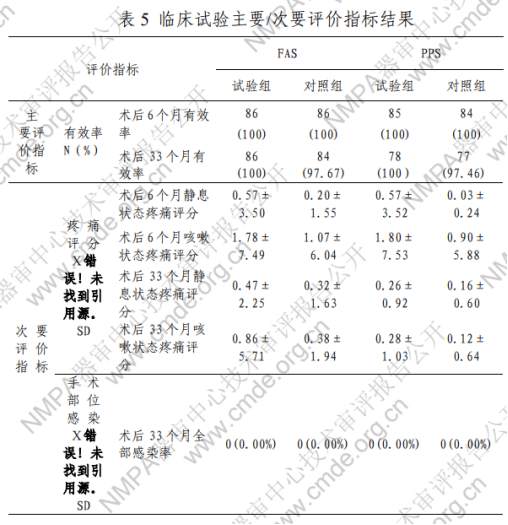

不良事件发生情况如表 7 所示。试验组与对照组之间,不良事件总数有统计学差异;不良事件发生率较高的 12/15 是手术部位的阳性 B 超检查结果,试验组发生率显著高于对 照组(P<0.05)。其余对照组和试验组不良事件发生率无统计 学差异。申请人对手术部位的阳性 B 超检查结果试验组发生 率高于对照组的情况进行了分析。患者无异常临床症状,其 他实验室检查无异常,认为阳性 B 超检查表现与生物材料植 入人体后降解与诱导组织再生有关,系生物材料植入人体后 组织再生过程的正常反应,无临床意义。与研究器械相关的 不良事件、严重不良事件、与研究器械相关的严重不良事件 发生率组间无统计学差异。
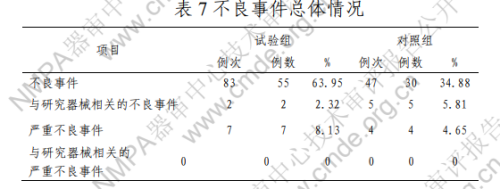
八)该产品在植入人体后对腹股沟疝缺损起到修补作 用,产品具有微孔支架结构,材料在降解过程中人体组织在 支架内部生长并修补缺损。相对于市场上已上市的生物补 片,产品还具有比表面积大和亲水性的特点,预期有助于患 者自体创伤愈合相关因子和细胞的粘附。但是,该类医疗器 械产品临床应用时也存在疝修补后复发、再次手术、组织免 疫反应、感染、疼痛、炎症、积液、血清肿、血肿等并发症 13/15 的风险。经综合评价,在目前认知水平上,认为该产品为患 者带来的受益大于风险。 为进一步观察产品在真实世界中的安全性和有效性,注 册人应在产品上市后进一步开展临床随访工作。
【关于我们】
南京西格玛医学技术股份有限公司,总部地处南京,业务覆盖全国。西格玛医学是一家专业从事医疗器械临床研究的创新型CRO,证券代码:873450,致力于为医疗器械提供临床试验专项服务、临床研究、方案撰写、统计分析、数据管理、临床监查、器械SMO、受试者招募、器械第三方稽查和器械注册申报的整体解决方案。
自2009年成立至今,先后更名为南京西格玛咨询中心,南京西格玛医药技术。多年评为江苏高新技术企业,江苏省医疗器械协会会员,通过ISO9001质量体系和多家国内外企业现场认证,和苏州大学,东南大学、南京医科大学成立联合工作站,已成功为遍布25个省份的国内外近千家客户提供专业技术服务,成功完成方案设计撰写、临床监查、数据管理、统计分析、稽查、注册申报等,并建立长期稳定的合作关系。涉及主要的30余个治疗领域,骨科、眼科、肾内科、护理部、整形外科、医疗美容、检验科、ICU、心内科,心外科,病理科、皮肤科等,与全国25个省份近千家医院开展合作,并在国内主要省市设立一站式服务,与全国80%的临床试验机构密切合作,拥有一支稳定并按照国内NMPA、国际标准(ICH-GCP)临床操作的专业团队,具有完整规范详细的标准操作规程(SOP),提供符合NMPA、FDA、EU MDR要求的试验及报告,成功完成NMPA医疗器械Ⅲ类产品临床试验1000余个。项目多次通过国家局、省局和外部审核和稽查。为更好服务和方便客户,我们在全国多个省市开设了上海南格分公司、北京、苏州、西安、长沙、广东等办事处。
【联系我们】
地址:江苏省南京市鼓楼区汉中路180号星汉大厦20楼AB座、CD座
电话:025-86210646
手机:同微信13585209568、13913960642
网址:http://www.sigma-stat.com/